Задание 17 из ЕГЭ по химии. Страница 5
Взаимодействие растворов нитрата серебра и бромида калия относится к реакциям
- замещения
- ионного обмена
- нейтрализации
- соединения
Взаимодействие гидроксида натрия с хлоридом меди(II) относят к реакциям
- соединения
- разложения
- замещения
- обмена
Реакция между магнием и муравьиной кислотой относится к реакциям
- соединения
- обмена
- разложения
- замещения
Взаимодействие гидроксида меди(II) с азотной кислотой относится к реакциям
- замещения
- соединения
- обмена
- окислительно-восстановительным
Какая из приведённых реакций не относится к реакциям ионного обмена?
- Ba(NO3)2 + Na2SO4 = BaSO4 + 2NaNO3
- КОН + HC1 = KC1 + H2O
- 2KMnO4 = K2MnO4 + MnO2 + O2
- Li2SO3 + 2HNO3 = 2LiNO3 +…
К реакциям обмена и замещения соответственно относятся взаимодействие
- серной кислоты с оксидом меди(II) и оксида натрия с оксидом углерода(IV)
- соляной кислоты с магнием и этена с …
Взаимодействие растворов хлорида бария и серной кислоты относится к реакциям
- соединения
- замещения
- обмена
- разложения
Взаимодействие между карбонатом кальция и соляной кислотой относится к реакциям
- соединения
- замещения
- нейтрализации
- обмена
Реакция, уравнение которой MgO(К) + CO2 (Г)→ MgCO3(К) + Q, относится к реакциям
- соединения, экзотермическим
- соединения, эндотермическим
- разложения, эндотермическим
- разложения, экз…
Взаимодействие этилена с бромоводородом является реакцией
- соединения, обратимой
- замещения, необратимой
- обмена, необратимой
- соединения, необратимой
При добавлении к раствору хлорида меди(II) порошка цинка при комнатной температуре протекает реакция
- присоединения
- обмена
- замещения
- нейтрализации
К реакциям обмена относится
- 2Al + Fe2O3 = 2Fe + Al2O3
- 2NaHCO3 = Na2CO3 + CO2 + H2O
- 2FeCl2 + Cl2 = 2FeCl3
- CrCl3 + 3NaOH = Cr(OH)3 + 3NaCl
К реакциям ионного обмена относится
- Ca + 2H2O = Ca(OH)2 + H2↑
- Na2CO3 + 2HNO3 = 2NaNO3 + H2O + CO2↑
- Mg + H2SO4 = MgSO4 + H2↑
- 3H2O + P2O5 = 2H3PO4
К реакциям обмена и соединения относятся соответственно
- C6H5OH + NaOH = C6H5ONa + H2O и 2Cu + O2 = 2CuO
- CH4 + Cl2 → CH3Cl + HCl и 2H2 + O2 = 2H2O
- 2SO2 + O2 ⇄ 2SO3 и K2SO3 + 2HCl =…
Химическая реакция, уравнение которой
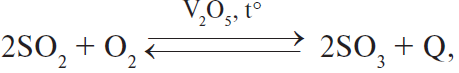
, является реакцией
- соединения, обратимой, некаталитической, эндотермической
- окислительно-восстановительной, обратимой, каталитической, экзо…
Реакция, уравнение которой
CuSO4 · 5H2O(ТВ.) = CuO(ТВ.) + SO3(Г.) + 5H2O(Г.) – Q,
относится к реакциям
- соединения, экзотермическим
- разложения, эндотермическим
- соединения, эндотерм…
Реакция, уравнение которой
CaCO3(ТВ.) = CaO(ТВ.) + CO2(Г.) – Q,
относится к реакциям
- соединения, экзотермическим
- разложения, эндотермическим
- соединения, эндотермическим
- разложения…
Реакции, обусловленные наличием π-связей в молекуле этилена, являются реакциями
- замещения
- присоединения
- обмена
- разложения
При нагревании нитрата железа(III) протекает реакция
- замещения
- обмена
- соединения
- разложения
Для реакций обмена нехарактерно
- выделение газообразного вещества
- образование малодиссоцирующего соединения
- образование нерастворимого вещества
- образование простого вещества





