Строение атома. Ядерные реакции. Законы радиоактивного распада
Физика атома
Атом — это наименьшая частица химического элемента, способная к самостоятельному существованию и обладающая его свойствами.
Каждому элементу соответствует определенный род атомов, обозначаемый химическим символом этого элемента. Например, атом кислорода обозначается символом О, атом водорода Н, атом гелия Не.
Атомы могут существовать в свободном состоянии (в виде отдельных атомов) в газах. В жидкостях и твердых телах они существуют в виде молекул, в которых соединяются с атомами того же элемента или других химических элементов (или, как принято говорить, существуют в связанном состоянии).
Со времен Демокрита (ок. 460—370 гг. до н. э.) и до конца XIX в. атом считался неделимой частицей — кирпичиком мироздания. После открытия электрона в 1897 г. английским ученым Дж. Дж. Томсоном стало ясно, что атом — сложная система.
Планетарная модель атома
С целью выяснения распределения положительного заряда в атоме английский ученый Э. Резерфорд исследовал рассеяние $α$-частиц фольгой из различных веществ. Большинство а-частиц беспрепятственно, почти без отклонений, проникало через фольгу, и только $1$ из $2000$ частиц отклонялась на углы, большие $90°$. В результате этих экспериментов в 1911 г. Резерфорд предложил следующую модель строения атома.
Атом состоит из положительно заряженного ядра, вокруг которого обращаются электроны, каждый на своей орбите, подобно планетам Солнечной системы, обращающимся вокруг Солнца. Поэтому модель называют планетарной.
Расстояние от электронов до ядра очень велико по сравнению с размерами ядра. Оценки Резерфорда показали, что диаметр ядра составляет порядка $10^{-12}—10^{-13}$ см. Размер самого атома $10^{-8}$ см. Положительный заряд ядра $q_{ядра}$ связан с числом электронов $Z$ в атоме соотношением:
$q_{ядра}=+Z·e$
где $е$ — заряд электрона.
Заряд ядра и число электронов в атоме, соответственно, совпадает с порядковым номером элемента в таблице Д. И. Менделеева.
В целом атом электронейтрален. При отрыве электрона от атома или присоединении электрона к атому (в результате столкновений, например, или при различных химических процессах) могут образоваться положительно или отрицательно заряженные ионы.
Простая и наглядная модель атома Резерфорда прекрасно объясняла результаты его опытов. Однако на основании этой модели нельзя объяснить факт существования атома, его устойчивость. Согласно законам электродинамики Максвелла электрон, движущийся по орбите с немалым ускорением, должен излучать электромагнитные волны с частотой, равной частоте его обращения вокруг ядра, в результате чего в скором времени, потеряв в результате излучения всю энергию, упасть на ядро. Согласно расчетам, основанным на механике Ньютона и электродинамике Максвелла, время это составляет всего $10^{-8}$ с. В действительности ничего подобного не происходит. Нейтральные невозбужденные атомы существуют неограниченно долго.
Это несоответствие опыта выводам теории связано с попыткой применения законов классической физики к внутриатомным явлениям (которые, как оказалось, подчиняются законам квантовой механики).
Выход из создавшейся в теории атома ситуации был найден датским физиком Нильсом Бором.
Состав ядра. Нуклонная модель Гейзенберга-Иваненко
Атомное ядро — это центральная часть атома, состоящая из протонов и нейтронов (которые вместе называются нуклонами).
Ядро было открыто Э. Резерфордом в 1911 г. при исследовании прохождения а-частиц через вещество. Оказалось, что почти вся масса атома ($99.95%$) сосредоточена в ядре. Размер атомного ядра имеет порядок величины $10^{-13}-10^{-12}$ см, что в $10 000$ раз меньше размера электронной оболочки.
Предложенная Э. Резерфордом планетарная модель атома и экспериментальное наблюдение им ядер водорода, выбитых $α$-частицами из ядер других элементов (1919—1920 гг.), привели ученого к представлению о протоне. Термин протон был введен в начале 20-х гг XX ст.
Протон (от protos — первый, символ $p$) — стабильная элементарная частица, ядро атома водорода.
Протон — положительно заряженная частица, заряд которой по абсолютной величине равен заряду электрона $e=1.6·10^{-19}$ Кл. Масса протона в $1836$ раз больше массы электрона. Масса покоя протона $m_p=1.6726231·10^{-27}кг=1.007276470 а.е.м.$
Второй частицей, входящей в состав ядра, является нейтрон.
Нейтрон (от лат. neuter — ни тот, ни другой, символ $n$) — это элементарная частица, не имеющая заряда, т. е. нейтральная.
Масса нейтрона в $1839$ раз превышает массу электрона. Масса нейтрона почти равна (незначительно больше) массе протона: масса покоя свободного нейтрона $m_n=1.6749286·10^{-27}кг=1.0008664902 а.е.м.$ и превосходит массу протона на $2.5$ массы электрона. Нейтрон, наряду с протоном под общим названием нуклон входит в состав атомных ядер.
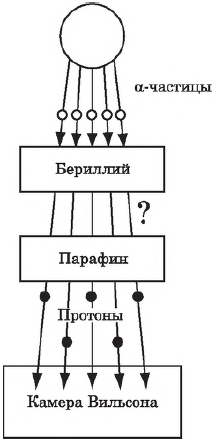
Нейтрон был открыт в 1932 г. учеником Э. Резерфорда Д. Чедвигом при бомбардировке бериллия $α$-частицами. Возникающее при этом излучение с большой проникающей способностью (преодолевало преграду из свинцовой пластины толщиной $10-20$ см) усиливало свое действие при прохождении через парафиновую пластину. Оценка энергии этих частиц по трекам в камере Вильсона, сделанная супругами Жолио-Кюри, и дополнительные наблюдения позволили исключить первоначальное предположение о том, что это $γ$-кванты. Большая проникающая способность новых частиц, названных нейтронами, объяснялась их электронейтральностью. Ведь заряженные частицы активно взаимодействуют с веществом и быстро теряют свою энергию. Существование нейтронов было предсказано Э. Резерфордом за 10 лет до опытов Д. Чедвига. При попадании $α$-частиц в ядра бериллия происходит следующая реакция:
$↙{4}↖{9}Be{+}{}↙{2}↖{4}He{→}{}↙{6}↖{12}C{+}{}↙{0}↖{1}n$
Здесь $↙{0}↖{1}n$ — символ нейтрона; заряд его равен нулю, а относительная атомная масса приблизительно равна единице. Нейтрон — нестабильная частица: свободный нейтрон за время $~15$ мин. распадается на протон, электрон и нейтрино — частицу, лишенную массы покоя.
После открытия Дж. Чедвиком нейтрона в 1932 г. Д. Иваненко и В. Гейзенберг независимо друг от друга предложили протоннонейтронную (нуклонную) модель ядра. Согласно этой модели, ядро состоит из протонов и нейтронов. Число протонов $Z$ совпадает с порядковым номером элемента в таблице Д. И. Менделеева.
Заряд ядра $Q$ определяется числом протонов $Z$, входящих в состав ядра, и кратен абсолютной величине заряда электрона $e$:
$Q=+Ze$
Число $Z$ называется зарядовым числом ядра или атомным номером.
Массовым числом ядра $А$ называется общее число нуклонов, т. е. протонов и нейтронов, содержащихся в нем. Число нейтронов в ядре обозначается буквой $N$. Таким образом, массовое число равно:
$A=Z+N$
Нуклонам (протону и нейтрону) приписывается массовое число, равное единице, электрону — нулевое значение.
Представлению о составе ядра содействовало также открытие изотопов.
Изотопы (от греч. isos — равный, одинаковый и topos — место) — это разновидности атомов одного и того же химического элемента, атомные ядра которых имеют одинаковое число протонов ($Z$) и различное число нейтронов ($N$).
Изотопами называются также ядра таких атомов. Изотопы являются нуклидами одного элемента. Нуклид (от лат. nucleus — ядро) — любое атомное ядро (соответственно атом) с заданными числами $Z$ и $N$. Общее обозначение нуклидов имеет вид $↙{A}↖{Z}X_N$, где $X$ — символ химического элемента, $A=Z+N$ — массовое число.
Изотопы занимают одно и то же место в Периодической системе элементов, откуда и произошло их название. По своим ядерным свойствам (например, по способности вступать в ядерные реакции) изотопы, как правило, существенно отличаются. Химические (и почти в той же мере физические) свойства изотопов одинаковы. Это объясняется тем, что химические свойства элемента определяются зарядом ядра, поскольку именно он влияет на структуру электронной оболочки атома.
Исключением являются изотопы легких элементов. Изотопы водорода $↖{1}H$ — протий, $↖{2}H$ — дейтерий, $↖{3}H$ — тритий столь сильно отличаются по массе, что и их физические и химические свойства различны. Дейтерий стабилен (т. е. не радиоактивен) и входит в качестве небольшой примеси ($1:4500$) в обычный водород. При соединении дейтерия с кислородом образуется тяжелая вода. Она при нормальном атмосферном давлении кипит при $101.2°$С и замерзает при $+3.8°$С. Тритий $β$-радиоактивен с периодом полураспада около $12$ лет.
У всех химических элементов имеются изотопы. У некоторых элементов имеются только нестабильные (радиоактивные) изотопы. Для всех элементов искусственно получены радиоактивные изотопы.
Изотопы урана. У элемента урана есть два изотопа — с массовыми числами $235$ и $238$. Изотоп $↙{92}↖{235}U$ составляет всего ${1}/{140}$ часть от более распространенного $↙{92}↖{238}U$.
Энергия связи нуклонов в ядре. Ядерные силы
Поскольку протоны в ядре имеют одинаковый положительный заряд, они отталкиваются. Для того чтобы удержать их вместе, должны существовать силы, намного превышающие силы электрического и гравитационного взаимодействия. Эти силы называются ядерными силами. Они в $100$ раз превосходят электрические (кулоновские) силы. Это самые мощные силы из всех, которыми располагает природа. Поэтому взаимодействие ядерных частиц относят к сильным взаимодействиям — особому типу взаимодействия, присущему большинству элементарных частиц наряду с электромагнитными взаимодействиями. Ядерные силы заметно проявляются лишь на расстояниях порядка $10^{-13}-10^{-12}$ см, равных по порядку величины размерам ядра, что показали опыты Резерфорда по рассеянию $α$-частиц ядрами.
Устойчивость атомного ядра характеризуется энергией связи ($Е_{св}$). Энергия связи — это энергия, которую надо затратить, чтобы расщепить ядро. Ее принято выражать в мегаэлектронвольтах (МэВ) ($1 МэВ = 1.6·10^{-13}Дж$).
Под энергией связи ядра понимают ту энергию, которая необходима для полного расщепления ядра на отдельные нуклоны. На основании закона сохранения энергии можно также утверждать, что энергия связи равна той энергии, которая выделяется при образовании ядра из отдельных частиц. Энергия связи атомных ядер очень велика. Определить ее можно, применяя соотношение Эйнштейна между массой и энергией: $E=mc^2$.
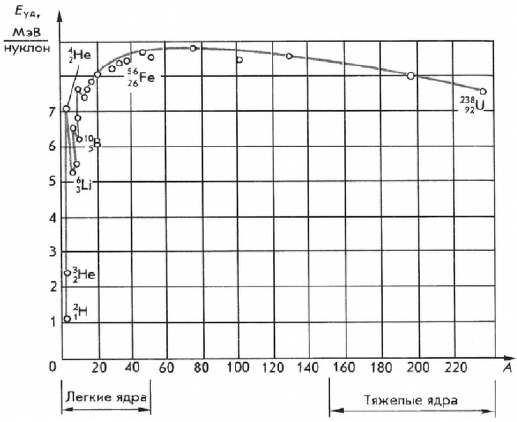
Удельной энергией связи называют энергию связи, приходящуюся на один нуклон ядра. Ее определяют экспериментально. Зависимость $Е_{уд}$ от массового числа $А$ приведена на рисунке. Как видно из рисунка, удельная энергия связи примерно постоянна (не считая самых легких ядер) и равна $8$ МэВ/нуклон. Слабый максимум ($8.6$ МэВ) приходится на элементы с массовыми числами от $50$ до $60$, т. е. на железо и близкие к нему по порядковому номеру элементы. Ядра этих элементов наиболее устойчивы.
У тяжелых ядер удельная энергия связи уменьшается за счет растущей с увеличением $Z$ кулоновской энергии отталкивания протонов. Кулоновские силы стремятся разорвать ядро.
Дефект массы
Точнейшие измерения показывают, что масса покоя ядра $М_я$ всегда меньше суммы масс покоя составляющих ее протонов и нейтронов: $М_я < Zm_p + Nm_n$. Существует положительная разность масс, называемая дефектом массы: $∆M=Zm_p + Nm_n-М_я$. Для гелия масса ядра на $0.75 %$ меньше суммы масс двух протонов и двух нейтронов. Для одного моля гелия $∆M=0.03$ г.
Уменьшение массы при образовании ядра из нуклонов означает, что при этом уменьшается энергия этой системы нуклонов на значение энергии связи $Е_{св}$:
$Е_{св}=∆Mc^2=(Zm_p + Nm_n-М_я)c^2$
Энергия связи переходит в энергию излучаемых при ядерных превращениях $γ$-квантов, которая равна как раз $Е_{св}$, и масса которых $∆M={Е_{св}}/{с^2}$.











